백시니아 바이러스 Vaccinia Virus (VACV)
재조합 VACV는 최대 25-30 kb의 큰 유전자 수용 능력과 넓은 tropism, 및 숙주 시스템에 의존하지 않는 복제 능력 등의 여러가지 장점이 있습니다. 최근 백신 개발 및 종양 치료를 포함한 광범위한 임상 응용 분야에서 높은 가능성을 보여주고 있습니다. VectorBuilder는 이제 in vitro 또는 in vivo 연구에 적합한 VACV 벡터의 클로닝 및 패키징 서비스를 모두 제공합니다.
VACV 서비스 제공 유형
- VAC-BAC backbone에 VACV vector cloning(약독화된 Western Reserve (WR) strain과 변형된 Vaccinia virus Ankara (MVA) strain에 적용 가능)
- VACV 바이러스 패키징
서비스 세부 사항
VACV BACYAC 벡터 클로닝
VectorBuilder는 VACV 벡터 복제를 위한 특허 벡터 백본 "BACYAC"를 개발했습니다. 이 백본은 박테리아 인공 염색체(BAC)와 효모 인공 염색체(YAC)의 핵심 요소를 결합했습니다. 백본의 BAC 요소는 벡터가 BAC처럼 행동하고 E. coli에서 전파되도록 허용하는 반면, YAC 요소는 벡터가 YAC처럼 행동하고 효모 Saccharomyces cerevisiae에서 전파되도록 합니다. 따라서 당사의 BACYAC 백본은 대장균 또는 효모에서 벡터를 성장 및 변형할 수 있는 유연성을 사용자에게 제공합니다. BACYAC 백본은 LacZ 또는 EGFP 리포터와 함께 사용할 수 있어 리포터 발현을 기반으로 감염된 세포를 쉽게 식별할 수 있습니다.
EGFP/LacZ 리포터 유전자, BACYAC 백본 및 백시니아 프로모터는 J2R site 사이의 백시니아 TK(thymidine kinase) 유전자에 삽입되어 약독화된 재조합 벡터를 제공합니다. MVA 및 약독화 WR 균주는 기초 연구, 전임상 및 임상 환경에서 사용할 수 있습니다. 우리는 또한 돌연변이를 통해 더 약독화된 바이러스를 생산할 수 있습니다.
VACV BACYAC 벡터의 기본 설계는 아래 Figure 1에 나와 있습니다.
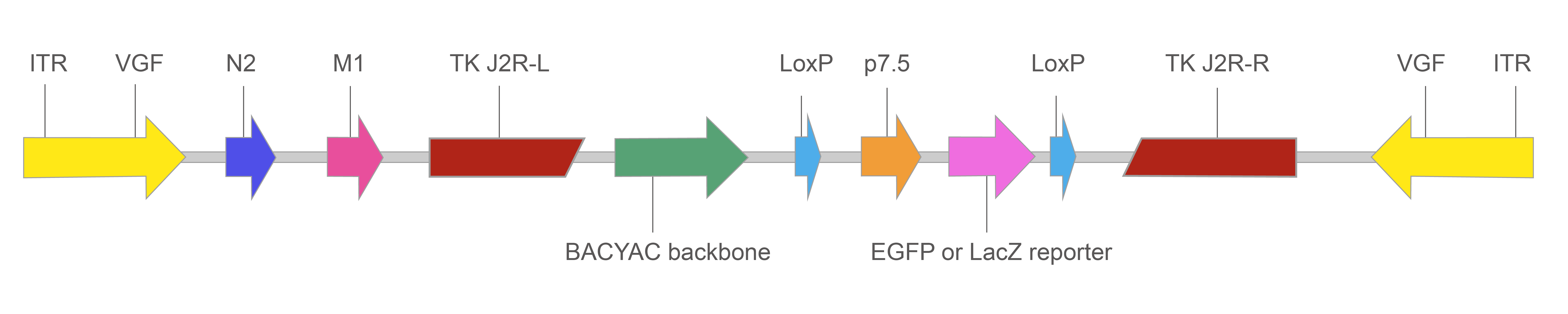
Figure 1. EGFP/LacZ 리포터가 포함된 재조합 VACV BACYAC 벡터의 맵.
TK: Thymidine kinase gene, 재조합 VACV에서 불활성화되어 약독화된 바이러스를 생성.
p7.5: Vaccinia promoter. 이 바이러스는 세포질에서 복제하기 때문에 백시니아 프로모터가 필요합니다. p7.5는 바이러스의 초기 및 후기 단계에서 전사적으로 활성화되기 때문에 일반적으로 도입유전자 발현을 유도하는 데 사용됩니다.
LoxP: Cre recombinase의 재조합 부위. Cre가 존재하면 두 개의 loxP 사이트 옆에 있는 영역이 절제됩니다
ITR: VGF(viral growth factor) 유전자를 포함하는 백시니아 게놈 측면의 Inverted terminal repeats.
N2: 숙주 면역 반응을 억제하는 초기 감염 동안 발현되는 유전자.
M1: 숙주 세포의 세포 사멸을 방지하여 바이러스 생산을 향상시키는 유전자.
EGFP 또는 LacZ 리포터: CMV 프로모터에 의해 구동되는 EGFP 또는 LacZ. 리포터 발현을 기반으로 감염된 세포를 쉽게 식별할 수 있습니다.
BACYAC 백본: Bacterial artificial chromosome (BAC) 및 yeast artificial chromosome (YAC) 백본. Chloramphenicol 내성 유전자를 이용한 E. coli와 His3 영양요구성 선별마커를 이용한 Saccharomyces cerevisiae에서 벡터를 선택적으로 증식할 수 있습니다.
VACV 바이러스 패키징
가격 및 소요 시간 Price Match
| Scale | Application | Titer | Volume | Price (USD) | Turnaround |
|---|---|---|---|---|---|
| Pilot |
Cell culture |
>108 PFU/ml | 250 ul (10x25 ul) | $399 | 21-28 days |
| Medium |
Cell culture |
>108 PFU/ml | 1 ml (10x100 ul) | $1,699 | 21-28 days |
| Ultra-purified medium | Cell culture & in vivo | >108 PFU/ml | 1 ml (10x100 ul) | $2,699 | 21-35 days |
배송 및 보관
VectorBuilder의 VACV는 HBSS buffer에 용해 후 드라이아이스로 배송됩니다. 수령 시 -80°C에서 장기간 보관(최소 6개월 이상 안정)하거나 -20°C에서 1주일 이내에 사용해야 합니다. VACV의 유효 기간은 약 1년입니다. 역가(titer)가 크게 떨어질 수 있으므로 VACV의 반복적인 동결-해동을 피하십시오.
기술적인 정보
VACV 생산 및 QC
바이러스 패키징 (Figure 2)은 목적유전자(GOI)를 운반하는 비감염성 VACV BACYAC plasmid를 포유류 세포에 transfection시키고 비복제성 helper바이러스인 fowlpox virus와 함께 감염시킵니다. VACV는 광범위한 숙주 세포를 감염시킬 수 있기 때문에 여러 세포주를 사용하여 재조합 바이러스를 패키징할 수 있습니다. VectorBuilder에서는 바이러스 제작 시 VACV 증폭에 다양한 세포주가 사용됩니다. VACV 증폭 단계 후 plaque 정제를 통해 추가로 증폭되는 바이러스 stock을 구축합니다. 세포외 외피바이러스(extracellular enveloped virus (EEV))와 세포내 성숙바이러스(intracellular mature virus (IMV))는 각각 상층액과 세포 용해물에서 회수됩니다. EEV는 PEG로 농축하고 IMV와 결합됩니다. Ultra-purified VACV의 경우 sucrose gradient purification으로 추가 정제됩니다.
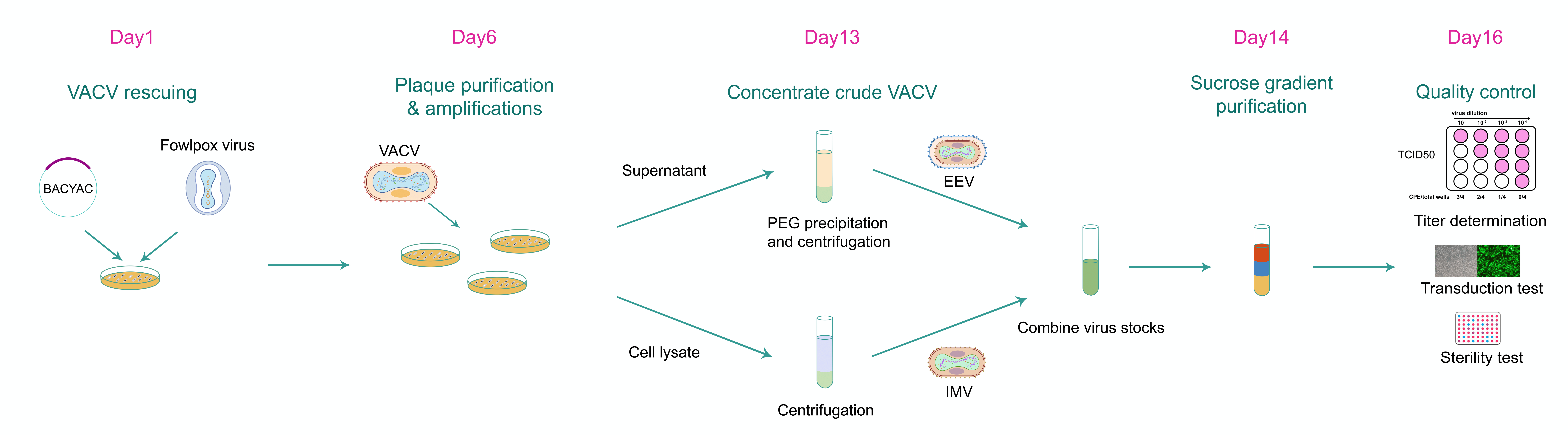
Figure 2. BACYAC vector로 VACV 패키징하는 일반적인 워크플로우.
VectorBuilder에서 생산된 각 재조합 VACV에 대한 품질 관리에는 titer 측정, 박테리아 및 곰팡이에 대한 무균 테스트, mycoplasma 검출이 포함됩니다. VACV 벡터가 형광단백질 또는 drug-selection 마커를 포함하는 경우 형광 검출 또는 drug selection으로 transduction 테스트를 수행합니다. Ultra-purified VACV의 경우 일반적으로 endotoxin assay를 수행하여 endotoxin level을 확인합니다. COA에 Endotoxin 결과를 포함시키는 것은 유상옵션입니다. 추가 QC 서비스는 요청 시 제공됩니다.
실험에 의한 검증
VectorBuilder의 성숙한 VACV는 완전히 검증되었으며 BHK21 세포주로 변환할 수 있는 것으로 나타났습니다 (Figure 3).
Before transduction After transduction
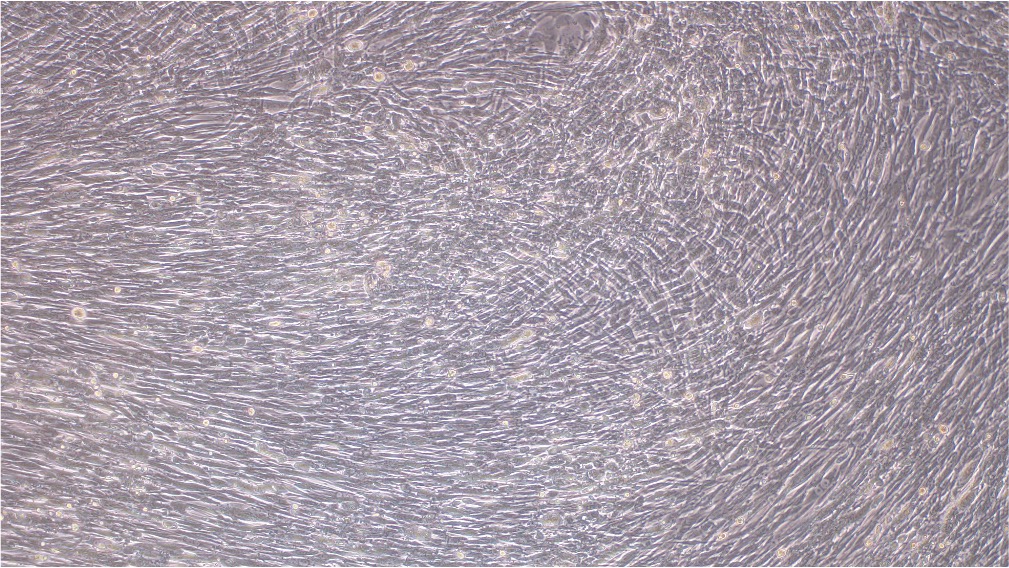

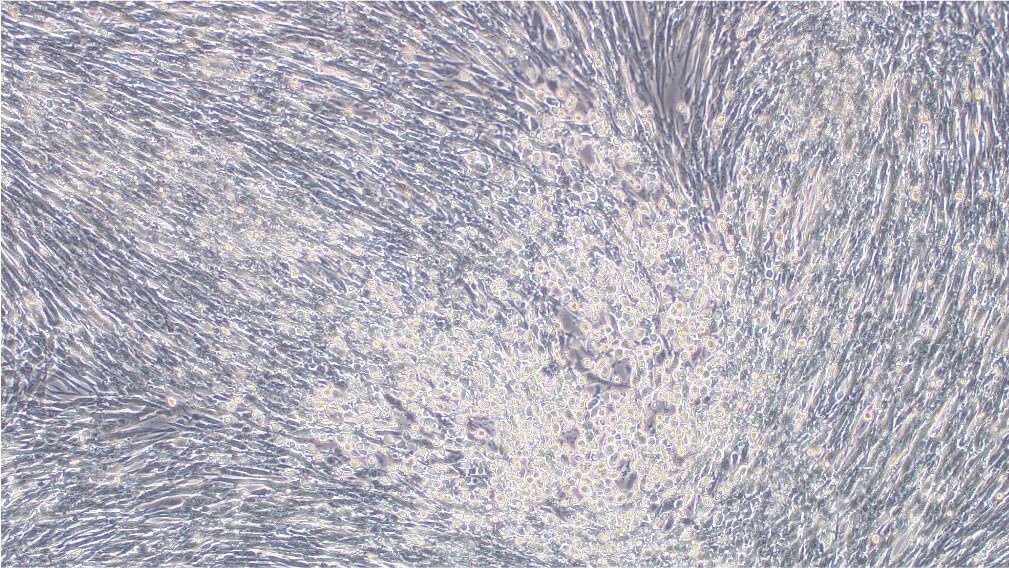
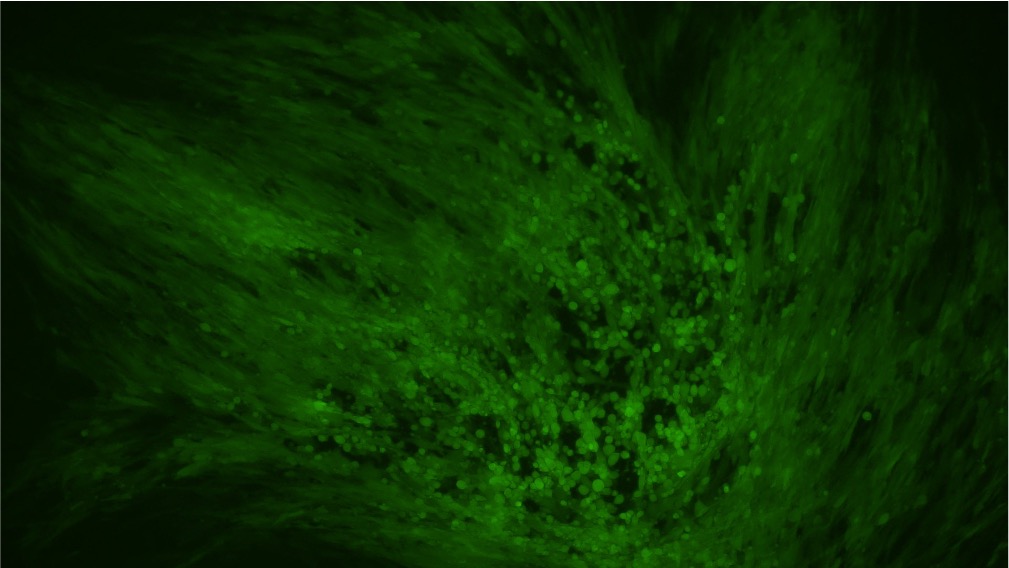
Figure 3. BHK21 세포가 MOI 0.5 일 때 EGFP 리포터를 포함한 BACYAC 벡터로 생산된 VACV로 형질도입 되었습니다. 변환 후 0시간 및 72시간에 이미지를 촬영했습니다. 배율: 100배. 왼쪽: bright field. 오른쪽: EGFP.
백시니아 배경
VACV는 poxvirus계열에 속하는 double-stranded linear DNA 바이러스입니다. 이 바이러스의 게놈 길이는 약 190kb이며 최대 25~30 kb의 외래유전자를 전달할 수 있습니다. 바이러스의 복제와 전사는 숙주 세포의 세포질에서 일어나며 바이러스 게놈은 DNA 복제와 RNA 전사에 필요한 모든 단백질을 암호화합니다. 따라서 바이러스의 생활사 동안 숙주 세포에 대한 의존도는 최소화됩니다.
바이러스의 초기 단계 시 많은 면역 조절 단백질이 생성되어 바이러스가 숙주의 선천적 항바이러스 방어에서 벗어나도록 돕습니다. 성숙한 VACV는 세포 용해 시 방출되는 intracellular mature virus (IMV)와 세포외 배출을 통해 세포에서 방출되는 extracellular enveloped virus (EEV)의 두 가지 주요 형태를 가집니다. 이 두 형태 모두 감염을 위한 숙주 세포 표면 수용체 결합 방법을 우회하여 지질막과 숙주 세포막의 융합을 통해 숙주 세포를 감염시킬 수 있습니다.
VACV 벡터의 주요 응용 분야
재조합 VACV 벡터는 다양한 유전자 치료 분야에 사용됩니다. VACV는 유리한 안전성과 큰 외래 유전자를 수용할 수 있는 능력, 광범위한 숙주 세포를 감염시킬 수 있는 능력, 그리고 바이러스 자체가 면역 표적이 되는 것을 방지하면서 숙주 면역 반응을 향상시키는 능력 등 많은 이점을 가진 유망한 시스템입니다.
다양한 수준의 감염성과 복제능을 가진 백시니아 계열의 다양한 균주가 개발되어 임상 분야 적용에 영향을 끼치고 있습니다. 가장 일반적인 균주로는 WR균주와 MVA균주가 있습니다. MVA는 약화형태로 인해 임상에 더 자주 사용되지만 WR은 복제 속도가 더 빠르고 숙주 면역 체계를 더 많이 조절할 수 있습니다. 두 변종은 현재 기초 연구와 임상 연구 모두에서 널리 사용되고 있습니다. 다음은 VACV가 사용된 주요 연구 분야 중 일부입니다:
암 치료
VACV는 암 세포를 용해시키는 직접적인 능력 외에도 간접적인 항종양 면역 반응을 유도하기 위해 사이토카인을 분비하는 면역세포를 모집하여 종양 미세 환경을 조절할 수 있습니다. 바이러스 고유의 이점을 유지하면서 안전성과 효능을 높이기 위해 특정 유전자 변형이 이루어집니다. 예를 들어, 종양 용해 바이러스인 Pexa-Vec은 TK 유전자의 결실을 통해 약독화되고 GM-CSF 이식 유전자를 발현하여 숙주 면역 반응을 증가시킵니다. 이 치료법은 다양한 고형암에 대한 임상 시험에서 사용되었습니다. 진행 중인 몇 가지 종양용해 VACV 임상시험은 종양용해요법을 위한 시스템으로서 VACV가 급속한 성장하고 있음을 보여줍니다.
백신 제작
VACV는 외부 항원 전달을 위한 유망한 플랫폼입니다. DNA 패키징 용량이 크고 천연두 백신으로 광범위하게 사용되어 왔기 때문에 HIV나 광견병을 포함한 다양한 병원균에 대한 백신을 만드는 데 이상적인 후보로 자리 잡았습니다.
유전자 치료에 VACV 사용의 장점
광범위한 친화성: VACV는 특정 receptor를 통해 세포로 도입되는 방식이 아니기 때문에 광범위한 세포를 감염시킬 수 있습니다.
게놈 삽입 위험 최소화: VACV의 생활사는 8시간으로 짧고 바이러스 복제가 세포질에서 일어나기 때문에 게놈 삽입의 위험을 제거했습니다.
종양 세포에서 높은 효능: VACV는 암세포를 선택적으로 감염시키고 고효율로 복제하여 종양 세포 용해를 유도하도록 설계할 수 있습니다.
독립적인 바이러스 복제: 바이러스는 mRNA 전사를 위한 숙주 시스템에 거의 의존하지 않으므로 숙주 세포의 생물학적 변화에 덜 영향을 받습니다.
숙주 면역 회피: VACV는 숙주 백혈구에 결합하여 비활성화시키는 백시니아 단백질의 분비와 숙주 외피 세포로 바이러스가 캡슐화되어 숙주 면역 체계를 회피할 수 있습니다. 따라서 VACV는 다양한 도입 방법을 통해 종양을 포함한 먼 거리의 타겟 조직까지도 전달할 수 있습니다.
대용량 유전자 전달 능력: VACV는 최대 30kb의 외래유전자를 수용할 수 있는 큰 게놈을 가지고 있습니다.
높은 바이러스 역가 및 전염성: VACV는 바이러스 역가가 높고 전염성이 높기 때문에 낮은 MOI로도 효율적인 형질도입을 할 수 있습니다.
주문 방법
자료
FAQ
VACV는 다음과 같은 몇가지 뚜렷한 장점을 제공합니다. 대용량 유전자 전달 능력, 다양한 분열 및 비분열 세포를 표적으로 삼을 수 있는 능력, 숙주 면역 시스템을 회피할 수 있는 능력, 세포질에서만 발생하는 바이러스 복제, 게놈 삽입 위험성 최소화 및 숙주 시스템 의존 감소. 다른 바이러스 유형과의 자세한 비교는 아래 표에서 확인 하십시오.
| Lentivirus | MMLV | Adenovirus | AAV | VACV | |
|---|---|---|---|---|---|
| Tropism | Broad | Broad | Ineffective for some cells | Depending on viral serotype | Broad |
| Carrying capacity | 6.4 kb | 5.5 kb | 7.5 kb | 4.2 kb | 25-30 kb |
| Can infect non-dividing cells? | Yes | No | Yes | Yes | Yes |
| Stable integration or transient | Stable integration | Stable integration | Transient, episomal | Transient, episomal | Transient, episomal |
| Maximum titer | High | Moderate | Very High | High | High |
| Promoter customization | Yes | No | Yes | Yes | No |
| Primary use | Cell culture and in vivo | Cell culture and in vivo | In vivo | In vivo | Cell culture and in vivo |
| Immune response in vivo | Low | Low | High | Very low | High |
VACV 벡터는 생바이러스를 직접 생산할 수 없지만, 생바이러스 생산을 위해 wild-type pox 바이러스에 감염된 패키징 세포에 트랜스펙션 할 수 있습니다. VectorBuilder는 안전하고 효율적으로 생산한 높은 역가를 위해 이 패키징 프로세스를 최적화했습니다.
VACV에는 생물안전 2등급 시설이 필요합니다.



