아데노부속바이러스 Adeno-Associated Virus (AAV) Packaging
재조합 아데노부속바이러스 (AAV)는 in vitro 및 in vivo 유전자 전달에 사용되는 다양하며 많이 사용되는 바이러스 벡터입니다. AAV는 다양한 포유류 세포 유형에 transduction할 수 있는 능력과 함께 인간에 대한 비병원성 및 낮은 면역원성 (immunogenicity) 때문에 유전자 치료에 가장 효과적인 수단 중 하나로 부상했습니다.
VectorBuilder는 AAV 기반 유전자 치료 실험을 지원하기 위해 최상의 품질의 AAV 패키징 서비스를 제공합니다. 당사는 특별히 벡터 클로닝 서비스에서 사용되는 AAV 벡터 시스템을 위해 titer, 순도, 효능 및 일관성 측면에서 재조합 AAV 생산 프로토콜을 크게 개선한 자체의 기술과 시약을 개발해왔습니다. 그 결과 고객의 AAV 벡터 클로닝과 AAV 패키징에 대한 요구를 만족시킴으로써 당사에 반복적으로 의뢰하는 고객들이 점점 많아지고 있습니다. 연구용 AAV 외에도 임상 응용을 위한 GMP-grade AAV 제조 서비스도 제공하고 있습니다.
제공되는 AAV 유형
- Single-stranded AAV (ssAAV) and self-complementary AAV (scAAV)
- Serotype 유형: 1, 2, 3, 4, 5, 6, 6.2, 7, 8, 9, rh10, PHP.eB, PHP.S, AAV2-retro, AAV2-QuadYF, AAV2.7m8, 등
- AAV empty capsids or virus-like particles (VLPs)
서비스 세부 사항
Research grade AAV 패키징
Research grade AAV 패키징 서비스는 기초 연구에서 AAV 기반 유전자 전달 니즈의 대부분을 충족합니다. 필요에 따라 triple transfection 및 baculovirus 기반 패키징 방법을 선택할 수 있습니다.
Triple Transfection-Based Approach
Baculovirus-Based Approach
가격 및 소요 시간 Price Match
| Scale | Application | Typical Titer | Minimum Titer | Volume | Price (USD) | Turnaround |
|---|---|---|---|---|---|---|
| Pilot | Non-purified, suitable for most cell culture experiments | >10 12GC/ml | >2x10 11 GC/ml | 250 ul (10x25 ul) | $449 |
6-12 days
|
| Medium | 1ml (10x100 ul) | $649 | ||||
| Large | >5x10 12 GC/ml | >2x10 12 GC/ml | 1ml (10x100 ul) | $1,099 | ||
| Ultra-purified pilot | Cell culture & in vivo | >2x10 13 GC/ml | >10 13 GC/ml | 100 ul (4x25 ul) | $1,399 |
7-14 days
|
| Ultra-purified medium | 500 ul (10x50 ul) | $1,999 | ||||
| Ultra-purified large | 1 ml (10x100 ul) | $3,099 | ||||
| Ultra-purified large 5 | 5 ml (10×500 ul) | From $9,899 | 14-21 days | |||
| Ultra-purified large 10 | 10 ml (10×1 ml) | From $15,899 | 21-28 days | |||
| Other scales | Please inquire | |||||
주:
1. GC = Genome copies.
2. Triple transfection에 의한 방법은 다음과 같은 serotype 에 대하여 가능합니다: 1, 2, 3, 4, 5, 6, 6.2, 7, 8, 9, rh10, DJ, DJ/8, PHP.eB, PHP.S, AAV2-retro, AAV2-QuadYF and AAV2.7m8.
3. AAV serotype 3, 4는 다른 serotype에 비해 titer가 낮습니다. 따라서 이들 serotype의 경우에는 위에 기재된 최소 역가(minimum titer)의 50%만을 보증합니다.
4. Ultra-purified scales의 경우 바이러스 입자는 cesium chloride (CsCl) density gradient centrifugation 에 의해 정제됩니다.
결과물
| For non-purified scales | For ultra-purified scales |
|---|---|
| Your custom AAV | Your custom AAV |
|
Free:non-purified control virus
|
Add-on purchase (optional):ultra-purified control virus
|
Control 바이러스
Control AAV는 맞춤형 바이러스의 생물학적 용도와 일치하도록 디자인되어, AAV transduction을 테스트하는 데 사용됩니다. 예를 들어 맞춤형 바이러스가 유전자를 과발현하는 경우, 제공되는 control 바이러스는 EGFP control AAV (EGFP 과발현 AAV)이고, 맞춤형 바이러스가 유전자에 대한 shRNA를 발현하는 것이면 제공된 control 바이러스는 scramble shRNA를 발현하는 것입니다. Control 바이러스에 대한 자세한 정보는 다음과 같습니다.
| 벡터 시스템 | Control 바이러스 벡터 이름 | Control 바이러스 벡터 ID |
|---|---|---|
| ssAAV 유전자 발현 시스템 | pAAV[Exp]-CAG>EGFP:WPRE | VB010000-9287ffw |
| scAAV 유전자 발현 시스템 | pscAAV[Exp]-CMV>EGFP | VB010000-9304aud |
| U6 기반의 shRNA knockdown ssAAV 시스템 | pAAV[shRNA]-CAG>EGFP-U6>Scramble_shRNA | VB010000-9489hhg |
| U6 기반의 shRNA knockdown scAAV 시스템 | pscAAV[shRNA]-EGFP-U6>Scramble_shRNA | VB010000-9343nhh |
| miR30 기반의 shRNA knockdown ssAAV 시스템 | pAAV[miR30]-CAG>EGFP:Scramble_miR30-shRNA:WPRE | VB010000-9494mnd |
Research plus grade AAV 패키징
Research plus AAV 패키징 서비스는 불순물(예: host cell protein, endotoxin 등)에 민감한 응용 분야이거나 또는 정제 방법, titer 또는 제형에 대한 특별한 요구 사항이 있는 응용 분야에 적합합니다. 또한 전임상 동물 실험을 위한 최적의 선택입니다.
가격 및 소요 시간 Price Match
| Scale | Application | Total Yield (GC) | Price (USD) | Turnaround |
|---|---|---|---|---|
| Research-plus 1 | Various in vitro & in vivo experiments | 1x10 13 | From $4,699 | 10-20 days |
| Research-plus 5 | 5x10 13 | From $14,899 | 21-28 days | |
| Research-plus 10 | 1x10 14 | From $23,899 |
주:
1. GC = Genome copies.
2.위에 기재된 가격 및 소요 시간은 CsCl density gradient centrifugation에 의한 정제를 기준으로 합니다. 다른 정제 방법(예: . iodixanol density gradient, affinity chromatography, ion-exchange chromatography 등) 이 필요한 경우 디자인 의뢰하기를 보내주시기 바랍니다.
| Scale | Application | Minimum Titer | Volume | Price (USD) | Turnaround |
|---|---|---|---|---|---|
| Ultra-purified pilot | Cell culture & in vivo | >5x10 13 GC/ml | 1 ml (10x100 ul) | $5,599 | 35-49 days |
| Ultra-purified medium | 5 ml (25x200 ul) | $20,199 | 35-49 days | ||
| Ultra-purified large | 10 ml (50x200 ul) | $38,199 | 35-49 days |
주:
1. GC = Genome copies.
2. Baculovirus에 의한 방법은 다음과 같은 serotype 에 대하여 가능합니다: 1, 2, 6, 8, 9.
3. Ultra-purified scales의 경우 바이러스 입자는 cesium chloride (CsCl) density gradient centrifugation 에 의해 정제됩니다.
결과물
| Your custom AAV |
|
Add-on purchase (optional):ultra-purified control virus
|
Control 바이러스
Control AAV는 맞춤형 바이러스의 생물학적 용도와 일치하도록 디자인되어, AAV transduction을 테스트하는 데 사용됩니다. 예를 들어 맞춤형 바이러스가 유전자를 과발현하는 경우, 제공되는 control 바이러스는 EGFP control AAV (EGFP 과발현 AAV)입니다. Control 바이러스에 대한 자세한 정보는 다음과 같습니다.
| 벡터 시스템 | Control 바이러스 벡터 이름 | Control 바이러스 벡터 ID |
|---|---|---|
| Baculovirus-AAV 혼성 유전자 발현 시스템 | pBV/AAV[Exp]-CMV>EGFP | VB200825-1105uwz |
배송 및 보관
Ultracentrifuge로 정제하지 않은 AAV는 Tris-based buffer에 저장되고, Ultracentrifuge로 정제한 AAV PBS-based buffer에 저장되어 있습니다. 당사의 AAV는 얼려서 드라이아이스와 함께 배송됩니다. 수령 즉시 장기보관을 위해 (최소 1년 이상 안정) -80℃에서 보관해야 하며, 2-3주 정도의 단기간내 사용시에는 -20℃에 보관하여야 합니다. 해동된 AAV 바이러스는 1-2주 동안 4 °C에서 보관할 수 있습니다. AAV는 다른 여러 바이러스들 (예: 렌티바이러스)보다 안정하며 여러번의 동결과 융해에도 바이러스 활성의 손실은 적지만, 실제로는 반복적인 동결-융해는 피하는 것이 좋습니다.
기술적인 정보
다양한 등급의 AAV 비교
아래 표는 연구용으로 제공되는 다양한 등급의 AAV 비교 입니다.
| Non-purified research grade | Ultra-purified research grade | Research plus grade | |
|---|---|---|---|
| Available purification method | - | CsCl density gradient | CsCl density gradient (default), iodixanol density gradient, affinity chromatography, ion-exchange chromatography |
| Titer | >10 12 GC/ml | >10 13 GC/ml | (1-5)x10 13 GC/ml |
| Achievable purity (assessed by SDS-PAGE) | - | >80% | >90% |
| Achievable endotoxin level | <30 EU/ml | <10 EU/ml | <2 EU/ml |
| Typical full capsid ratio | - | >70% | >80% |
AAV 제조 및 QC
Triple Transfection-Based Approach
Baculovirus-Based Approach
VectorBuilder의 재조합 AAV를 제조하기 위하여 목적 유전자(GOI)를 운반하는 transfer plasmid와 함께 AAV 복제를 매개하는 당사 전유의 Rep-cap plasmid와 아데노바이러스 유전자들 E4, E2A, VA를 인코딩하는 helper plasmid를 HEK293T 패키징 세포주에 co-transfection 합니다. 짧은 배양기를 거친 뒤 serotype에 따라 세포 용해물 (lysate) 또는 상청액에서 바이러스 입자를 채취하여 PEG precipitation에 의해 농축합니다. Ultracentrifuge에 의해 정제되는 AAV (in vivo grade) 의 경우 바이러스 입자를 cesium chloride (CsCl) gradient ultracentrifugation에 의해 더욱 정제하고 농축합니다. 당사는 qPCR에 의하여 AAV titer를 측정합니다.
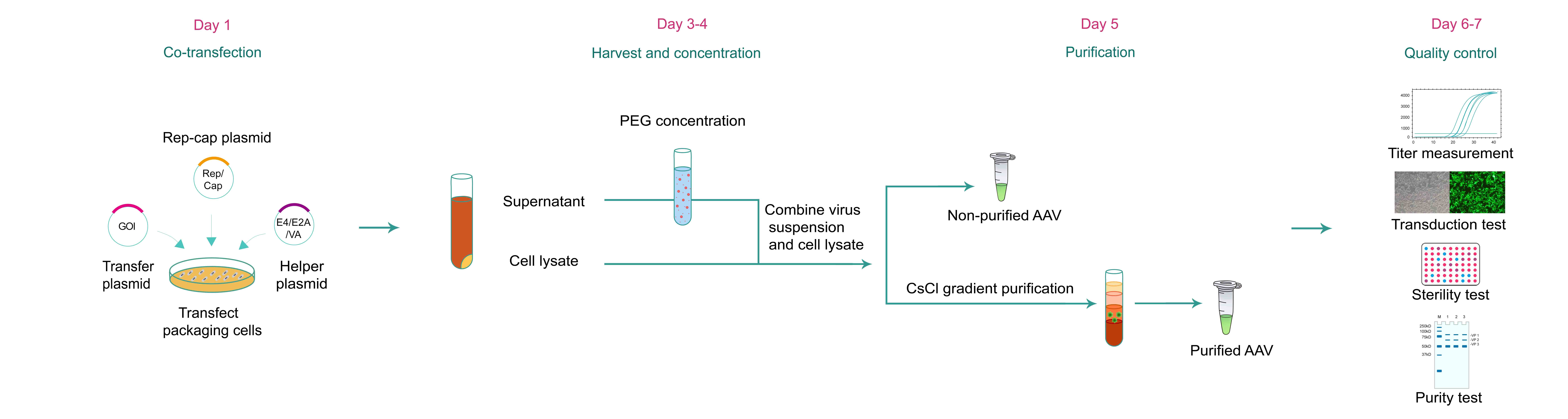
Figure 1. Triple transfection에 의한 AAV 패키징의 전형적인 워크플로우
VectorBuilder에서 생산되는 각각의 AAV에 대한 품질관리에는 titer 측정, 박테리아 및 fungi에 대한 무균 테스트, mycoplasma 검출 등이 있습니다. Transfer 벡터가 형광 단백질을 인코딩하는 경우, 해당 형광을 검출하기 위해 transduction 테스트를 수행합니다. 추가로 ultracentrifuge에 의해 정제된 AAV의 경우, SDS-PAGE 분석 및 endotoxin 분석을 통해 virus 품질을 체크합니다. 고객맞춤형 연구 니즈를 충족시키기 위해 보다 엄격한 QC 서비스를 추가로 제공할 수 있습니다.
아래 표는 VectorBuilder에서 제공할 수 있는 QC 서비스입니다.
AAV 제조 및 QC
배큘로바이러스 (baculovirus) 기반의 AAV 패키징 워크플로우는 아래 Figure 1에서와 같이 두가지 주요 단계로 구성됩니다. Step 1은 두 종류의 재조합 배큘로바이러스를 만드는 단계로, 관심 유전자 (GOI)와 GOI 양쪽에 있는AAV inverted terminal repeats (ITRs)를 발현하는 첫번째 배큘로바이러스와, AAV rep 및 cap 유전자를 발현하는 두번째 helper 배큘로바이러스를 제조합니다. Step 2에서는 Step 1에서 생성된 두 종류의 재조합 배큘로바이러스를 곤충 세포에 함께 감염시켜서 재조합 AAV를 생성합니다.
두 종류의 재조합 배큘로바이러스 (관심 유전자 (GOI)와 GOI 양쪽에 있는AAV inverted terminal repeats (ITRs)를 발현하는 바이러스와 AAV rep/cap 유전자를 발현하는 바이러스)를 생성하기 위해, 각 배큘로바이러스에 대한 발현 카세트는 먼저 배큘로바이러스 transfer 벡터에 클로닝됩니다. 배큘로바이러스 transfer plasmid는 Tn7 transposase를 발현하는 helper plasmid와 함께 empty 배큘로바이러스 shuttle 벡터 (a.k.a. bacmid)가 들어있는 박테리아 숙주로 co-transformation되어 재조합 bacmid를 생성합니다. 그런 다음 재조합 bacmid는 곤충세포 Sf9으로 transfection됩니다. 짧은 인큐베이션 기간 후, 바이러스 입자를 배지에서 수확하고, sucrose cushion centrifugation에 의해 추가로 농축합니다. 배큘로바이러스 titer를 측정하기 위해서 qPCR 방법을 사용합니다. 그 다음에 두 재조합 배큘로바이러스는 곤충 세포에 co-infection됩니다. 72-96 시간의 인큐베이션 후, AAV 입자는 세포의 lysate와 상청액으로부터 수확되고 PEG precipitation에 의해 농축됩니다. Ultracentrifuge에 의해 정제되는 AAV (in vivo grade)의 경우 바이러스 입자는 cesium chloride (CsCl) gradient ultracentrifugation에 의해 추가로 정제되고 농축됩니다. AAV titer는 qPCR 방법을 사용하여 측정됩니다.
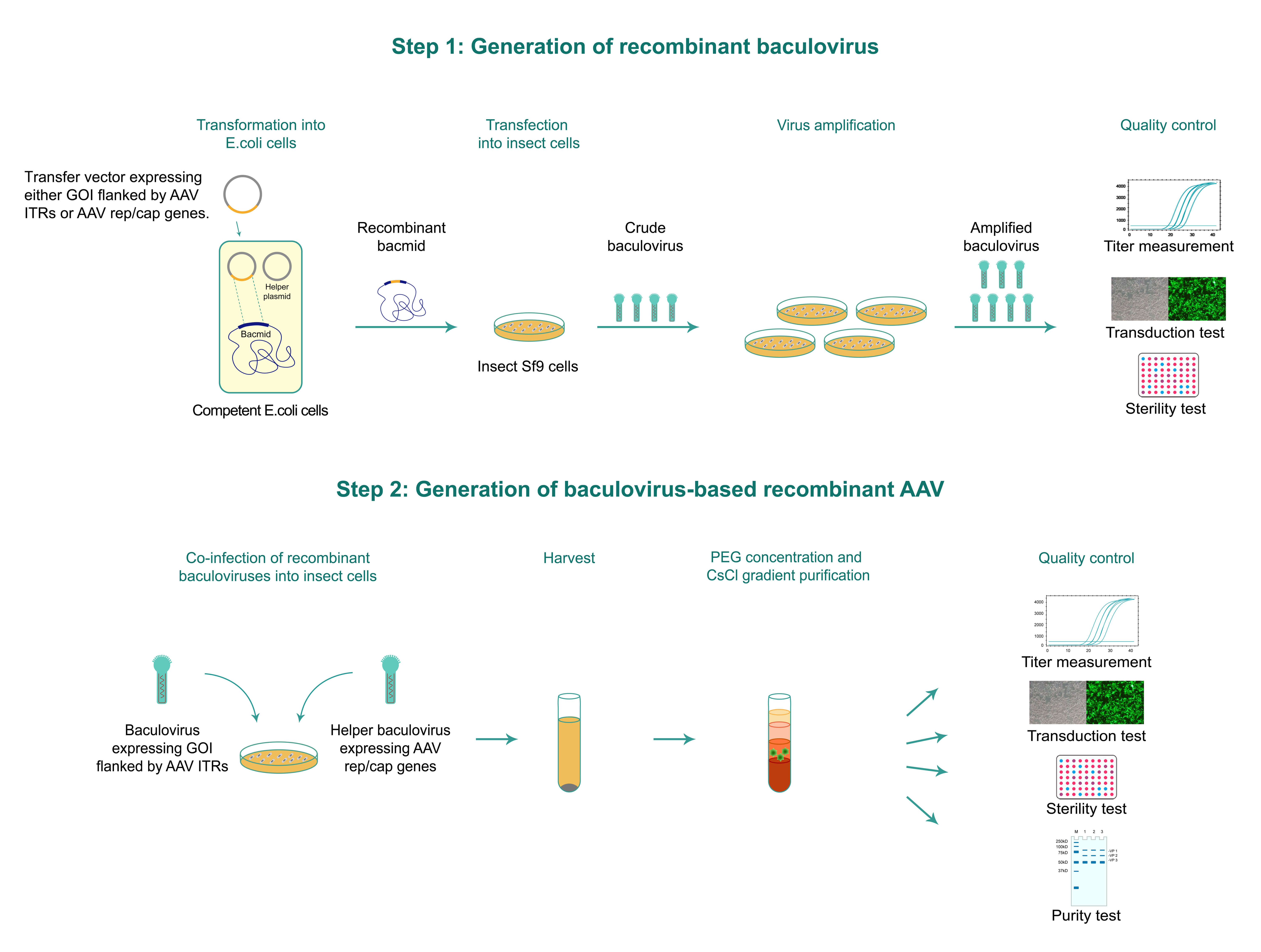
Figure 1. Baculovirus에 의한 AAV 패키징의 전형적인 워크플로우
VectorBuilder에서 생산되는 각각의 AAV에 대한 품질관리에는 titer 측정, 박테리아 및 fungi에 대한 무균 테스트, mycoplasma 검출 등이 있습니다. Transfer 벡터가 형광 단백질을 인코딩하는 경우, 해당 형광을 검출하기 위해 transduction 테스트를 수행합니다. 추가로 ultracentrifuge에 의해 정제된 AAV의 경우, SDS-PAGE 분석 및 endotoxin 분석을 통해 virus 품질을 체크합니다.
| Other QC services | Methods |
|---|---|
| Endotoxin testing | LAL |
| Titer determination | ddPCR |
| TCID50 | |
| Replication-competent AAV testing | qPCR |
| Empty capsid analysis | TEM |
| CDMS | |
| SV-AUC |
권장하는 AAV serotype
Serotype에 따른 목록
Tissue 유형에 따른 목록
| Serotype | Tissue tropism |
|---|---|
| AAV1 | Smooth muscle, skeletal muscle, CNS, lung, retina, inner ear, pancreas, heart, liver |
| AAV2 | Smooth muscle, CNS, liver, kidney, retina, inner ear |
| AAV3 | Smooth muscle, liver, lung |
| AAV4 | CNS, retina, lung, kidney |
| AAV5 | Smooth muscle, CNS, lung, retina |
| AAV6 | Smooth muscle, heart, lung, adipose, liver |
| AAV6.2 | Lung, liver, inner ear |
| AAV7 | Smooth muscle, retina, CNS, liver |
| AAV8 | Smooth muscle, CNS, retina, inner ear, liver, pancreas, heart, kidney, adipose |
| AAV9 | Smooth muscle, skeletal muscle, lung, liver, heart, pancreas, CNS, brain, retina, inner ear, testes, kidney |
| AAV-rh10 | Smooth muscle, lung, liver, heart, pancreas, CNS, retina, kidney |
| AAV-DJ | Liver, heart, kidney, spleen |
| AAV-DJ/8 | Liver, brain, spleen |
| AAV-PHP.eB | CNS |
| AAV-PHP.S | PNS |
| AAV2-retro | Spinal nerves |
| AAV2-QuadYF | Endothelial cell, retina |
| AAV2.7m8 | Retina, inner ear |
| Tissue type | Recommended AAV serotypes |
|---|---|
| Smooth muscle | AAV1, AAV2, AAV3, AAV5, AAV6, AAV7, AAV8, AAV9, AAV-rh10 |
| Skeletal muscle | AAV1, AAV9 |
| CNS | AAV1, AAV2, AAV4, AAV5, AAV7, AAV8, AAV9, AAV-rh10, AAV-PHP.eB |
| PNS | AAV-PHP.S |
| Brain | AAV1, AAV2, AAV5, AAV7, AAV8, AAV9, AAV-DJ/8 |
| Retina | AAV1, AAV2, AAV4, AAV5, AAV7, AAV8, AAV9, AAV-rh10, AAV2-QuadYF, AAV2.7m8 |
| Inner ear | AAV1, AAV2, AAV6.2, AAV8, AAV9, AAV2.7m8 |
| Lung | AAV1, AAV3, AAV4, AAV5, AAV6, AAV6.2, AAV9, AAV-rh10 |
| Liver | AAV1, AAV2, AAV3, AAV6, AAV6.2, AAV7, AAV8, AAV9, AAV-rh10, AAV-DJ, AAV-DJ/8 |
| Pancreas | AAV1, AAV2, AAV6, AAV8, AAV9, AAV-rh10 |
| Heart | AAV1, AAV4, AAV5, AAV6, AAV8, AAV9, AAV-rh10, AAV-DJ |
| Kidney | AAV2, AAV4, AAV8, AAV9, AAV-rh10, AAV-DJ, AAV-DJ/8 |
| Adipose | AAV6, AAV8, AAV9 |
| Testes | AAV2, AAV9 |
| Spleen | AAV-DJ, AAV-DJ/8 |
| Spinal nerves | AAV2-retro |
| Endothelial cells | AAV2-QuadYF |
* 목적 유전자(GOI)를 운반하는 ITR은 AAV2 유전체에서 가져온 것입니다. capsid 단백질의 serotype에 의하여 AAV의 serotype이 구별됩니다.
각 AAV serotype에 대한 major viral capsid protein 1 (VP1)의 아미노산 서열을 원하시면 여기를 눌러주십시요. >>실험적인 검증
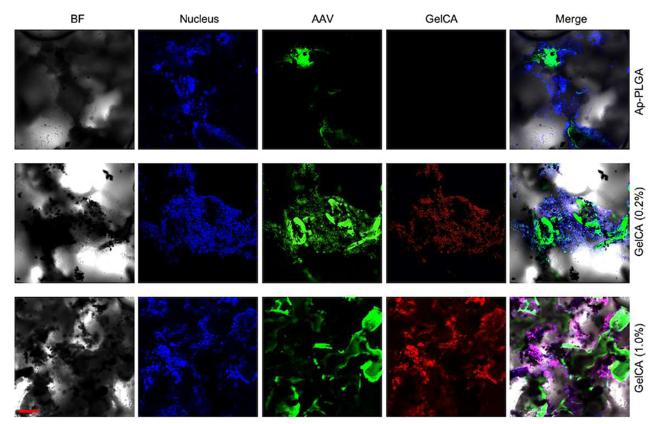
VectorBuilder는 배큘로바이러스에 의한 AAV 패키징 프로토콜을 최적화하기 위해 여러 자체적인 기술을 개발했으며, 당사에서 제조된 바이러스는 포유류 세포에서 높은 transduction효율을 나타내는 것으로 검증되었습니다.
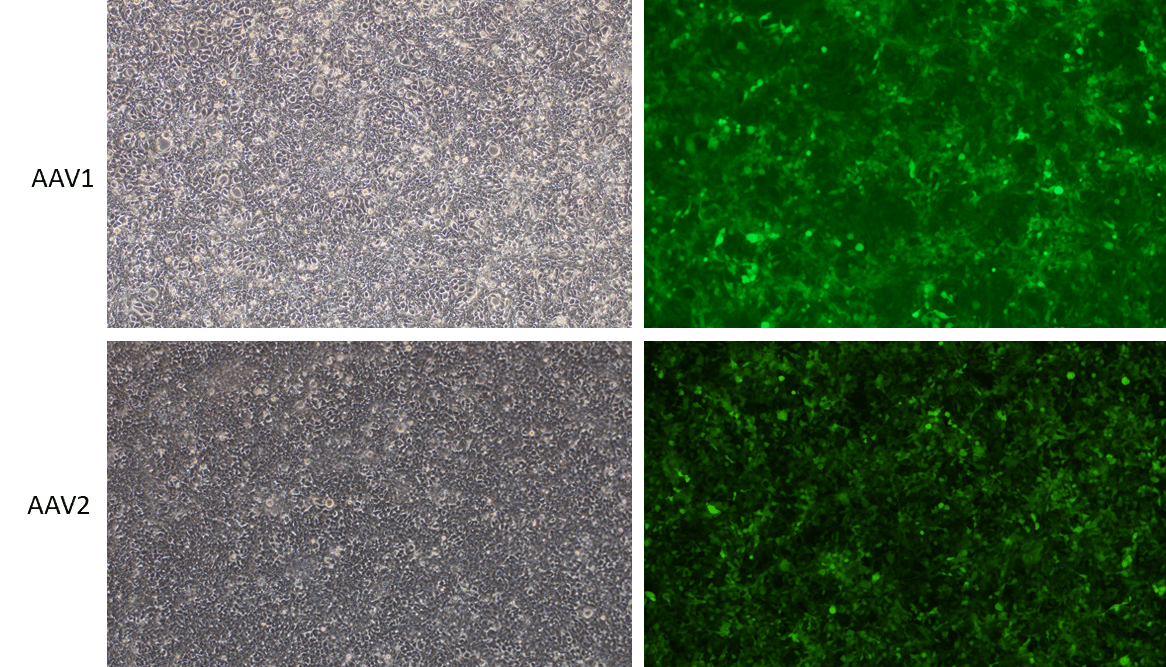
Figure 2. Baculovirus에 의해 제조된 EGFP를 발현하는 AAV1과 AAV2를 각각 293T 세포에 MOI 10000으로 transduction한 결과입니다. 배율: 100x. 왼쪽: bright field. 오른쪽: GFP.
실험에 의한 검증
VectorBuilder는 triple transfection-based AAV packaging 프로토콜을 최적화하기 위해 여러 독점 기술을 개발했으며 당사 바이러스는 포유류 세포에서 높은 형질도입 효율을 나타내는 것으로 검증되었습니다.
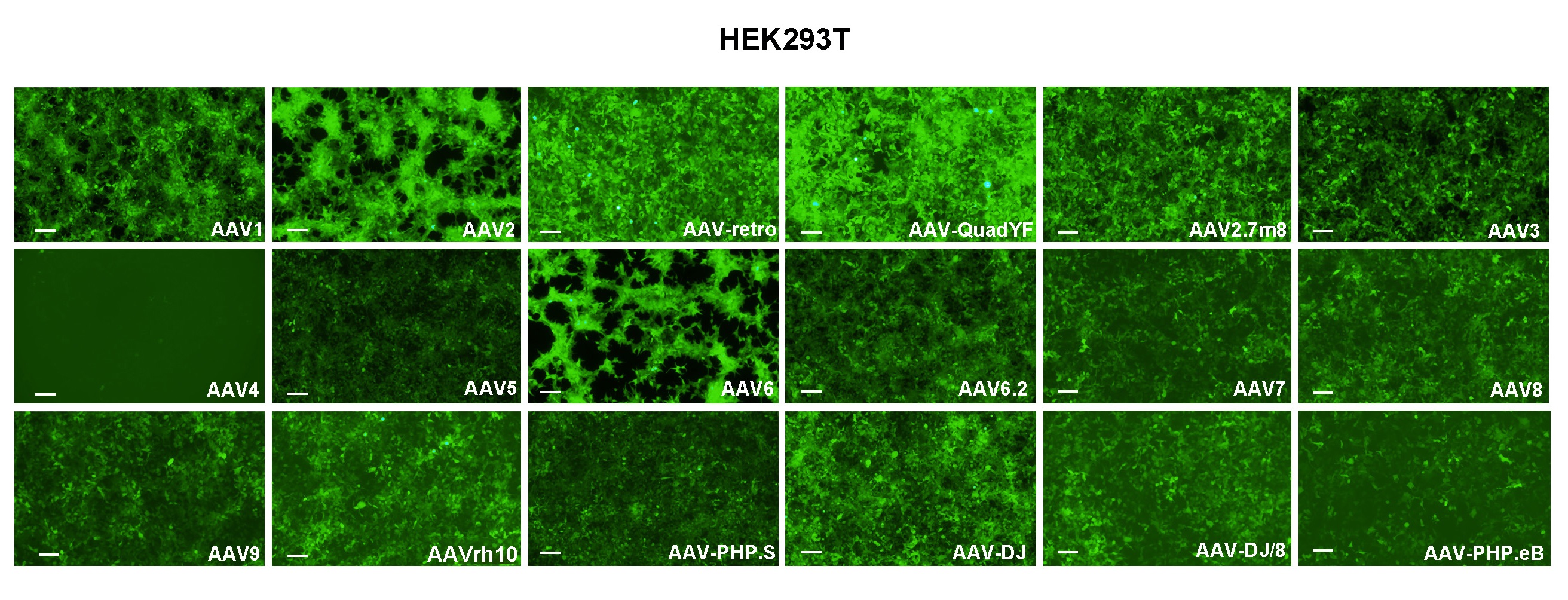
Figure 2.HEK293T cells were transduced with 18 serotypes of recombinant AAV packaged from the same CMV>EGFP vector ( VB010000-9394npt). Representative EGFP expression at 48 h post transduction in different serotypes is shown as indicated. Scale bars: 100 μm.
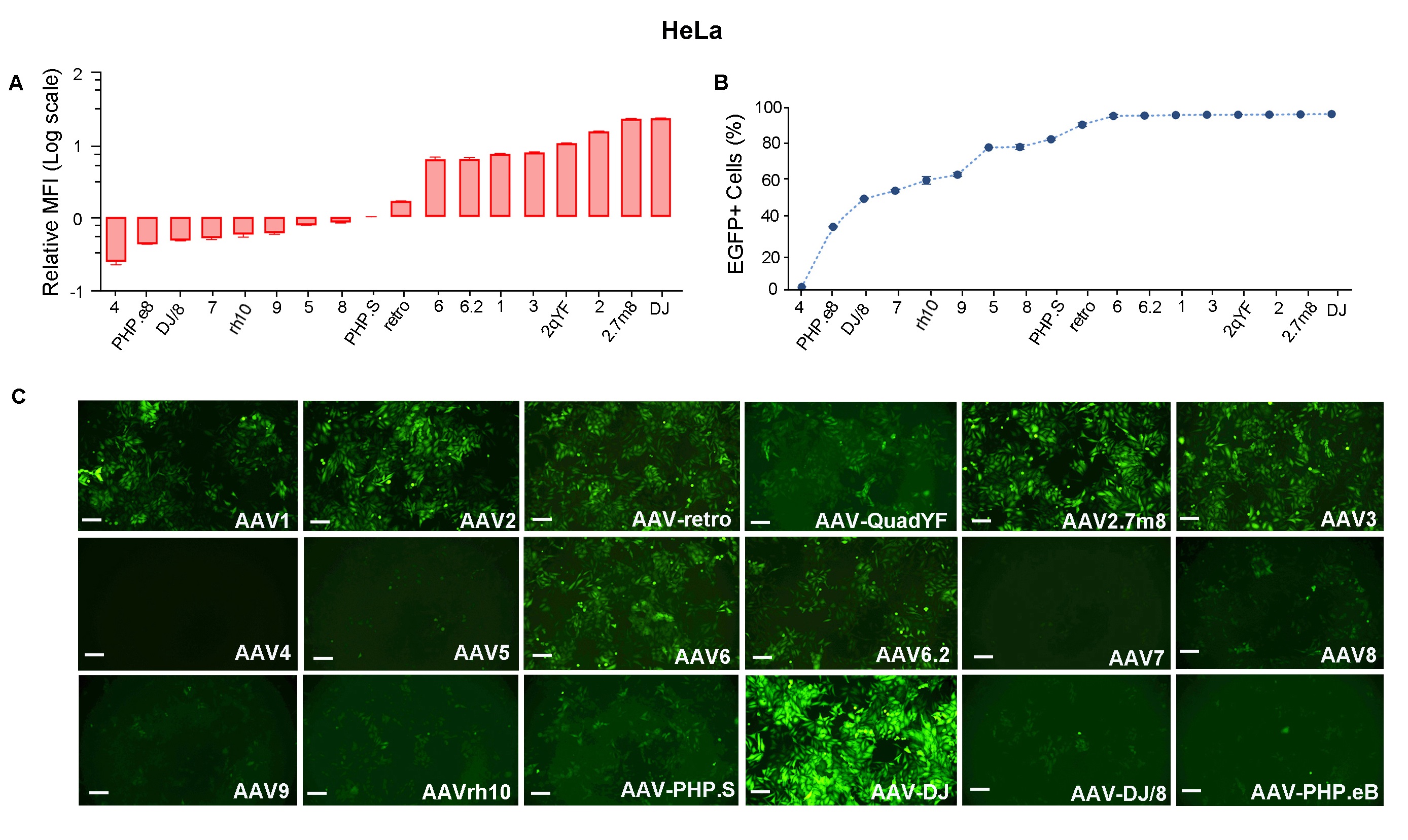
Figure 3.HeLa cells were transduced with 18 serotypes of recombinant AAV packaged from the same CMV>EGFP vector ( VB010000-9394npt). EGFP (A) Mean Fluorescence Intensity (MFI) and (B) positivity were quantified using flow cytometry 48 h post transduction. (C) Representative EGFP expression in different serotypes is shown as indicated. Scale bars: 100 μm.
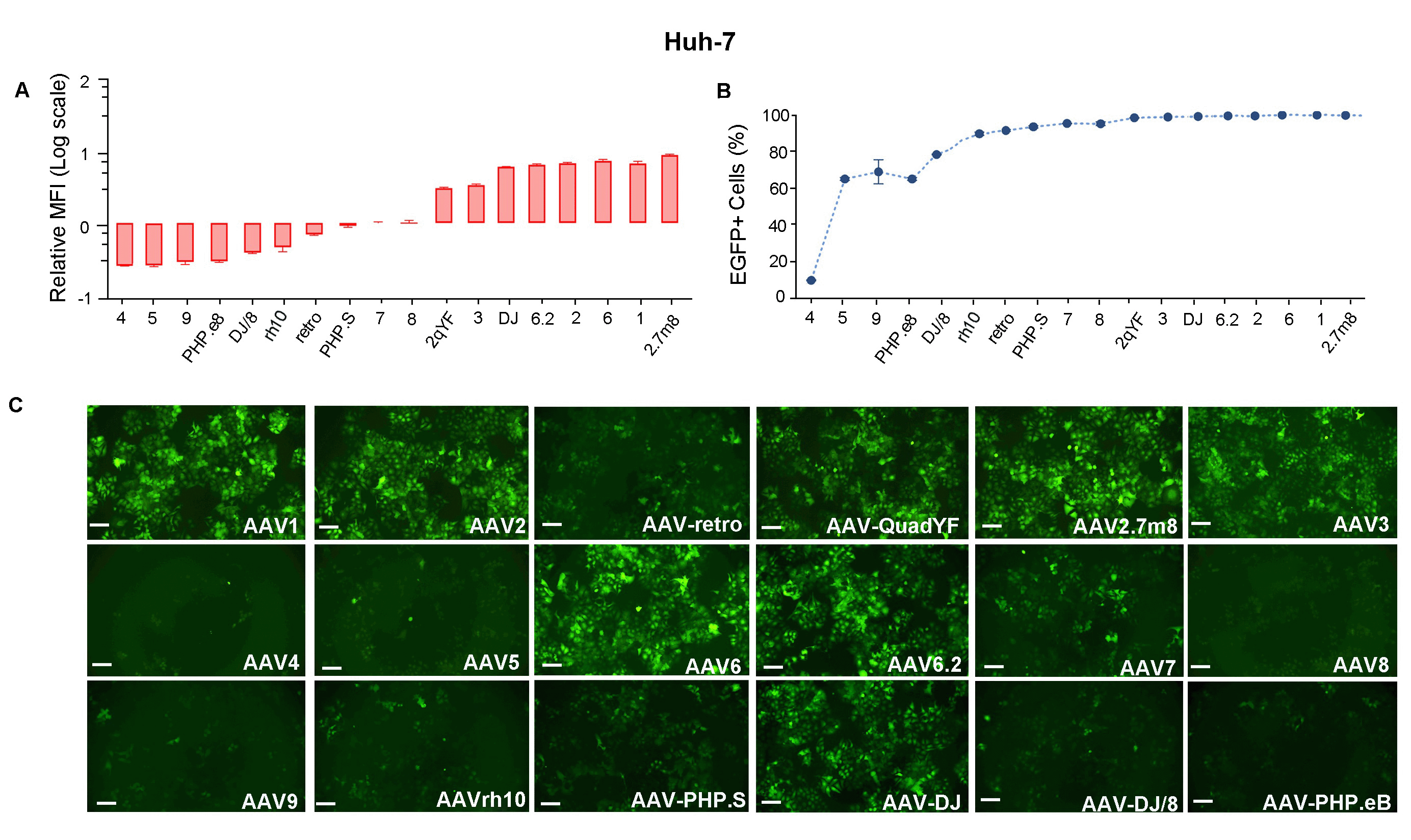
Figure 4.Huh-7 cells were transduced with 18 serotypes of recombinant AAV packaged from the same CMV>EGFP vector ( VB010000-9394npt). EGFP (A) Mean Fluorescence Intensity (MFI) and (B) positivity were quantified using flow cytometry 48 h post transduction. (C) Representative EGFP expression in different serotypes is shown as indicated. Scale bars: 100 μm.
주문 방법
고객이 제공하는 벡터
고객이 제공하는 AAV 벡터를 사용하여 패키징하는 경우 시료 제출 가이드라인에 따라서 벡터를 보내주시기 바랍니다. 배송 지연이나 시료 손상을 방지하기 위해 당사의 가이드라인을 엄격히 따라 주시기 바랍니다. 모든 고객이 제공하는 시료는 VectorBuilder에 의해 의무적으로 QC를 거치며 각 품목에 대해 $100의 추가 요금이 부과될 수 있습니다. 고객이 제공한 시료가 QC를 통과할 때까지는 생산을 시작할 수 없음을 유의하시기 바랍니다.
자료
문서 자료
사용 설명서 물질안전보건자료 (MSDS) 시험성적서 (COA) 소책자 & 브로셔자주 묻는 질문
| 렌티바이러스 | MMLV | 아데노바이러스 | AAV | |
|---|---|---|---|---|
| Tropism (친화성) | Broad | Broad | 어떤 세포들에는 비효율적임 | 바이러스 serotype (혈청형)에 따라서 다름 |
| 분열하지 않는 세포에 감염이 가능한가? | Yes | No | Yes | Yes |
| 호스트 유전체에 안정한 결합을 하는가 아니면 단기적인가? | Stable integration | Stable integration | Transient, episomal | Transient, episomal |
| 최대 titer | High | Moderate | High | Very high |
| 맞춤형 promoter | Yes | No | Yes | Yes |
| 주요 용도 | Cell culture and in vivo | Cell culture and in vivo | In vivo | In vivo |
| In vivo에서의 면역반응 | Low | Low | High | Very low |
VectorBuilder에서는 AAV의 titer를 측정하기 위하여 먼저 용해시킨 바이러스 입자로부터 유전체를 추출합니다. 그 다음에 qPCR 을 사용하여 ITR 서열의 copy 수를 정확히 측정하여 이로부터 바이러스 유전체의 copy 수를 정량합니다. 추가 비용으로 ddPCR, TCID50 등에 의한 다른 titration 서비스도 제공합니다.
당사에 의하여 보장되는 titer는 패키징 되는 5’ ITR에서 3’ ITR까지의 영역이 AAV cargo limit (4.7 kb) 이하일 때 적용됩니다. 그 이상의 경우 패키징되는 서열에 절단이 일어나서 기능성을 상실할 수 있습니다. 또한 다음과 같은 경우 titer를 보장해드릴 수 없습니다.
- AAV serotype 3, 4, 6, 6.2 및 2.7m8 은 다른 serotype에 비해 titer가 낮습니다. 따라서 이들 serotype의 경우에는 표준 최소 역가의 50%만을 보증합니다.
- Proapoptotic 유전자와 같이 숙주 세포에 대한 독성을 나타낼 수 있는 유전자들, 세포막 단백질과 같이 세포들이 응집하게 만들어서 세포나 바이러스의 integrity를 손상시킬 수 있는 유전자들과 같이 패키징 과정에 유해한 작용을 할 수 있는 서열들이 포함되어 있거나, 반복 서열 또는 GC 함량이 매우 높아서 재배열이나 2차 구조를 만들 가능성이 높은 서열을 포함하는 벡터들.
- 고객이 벡터를 제공하는 경우 벡터 품질에 대한 컨트롤이 없거나 당사의 패키징 시스템과 호환되지 않으면 titer를 보증할 수 없습니다.
예상 소요 시간은 제조 시작부터 완료까지의 시간을 의미합니다. 고객이 제공한 시료 (template DNA나 바이러스 벡터 등)의 운송 시간과 QC, 최종 결과물을 고객에게 배송하기 위한 운송 시간은 포함되지 않습니다.